Khối lượng khí thoát ra
Phương trình trạng thái khí lí tưởng:
Khối lượng khí thoát ra
Phương trình trạng thái khí lí tưởng:
Chia sẻ qua facebook
Hoặc chia sẻ link trực tiếp:
www.congthucvatly.com/cong-thuc-khoi-luong-da-bay-ra-khi-thay-doi-trang-thai-vat-ly-10-830
V
Khái niệm:
V là thể tích của lượng khí đang xét.
Đơn vị tính: lít (l)
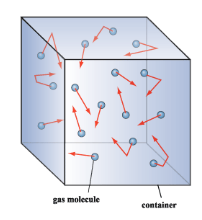
p
Khái niệm:
Áp suất chất khí thường được dùng để chỉ lực trung bình trên một đơn vị diện tích được tác động lên bề mặt của bình chứa.
Đơn vị tính: Pascal (Pa)
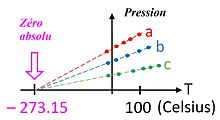
T
Khái niệm:
- Nhiệt độ không tuyệt đối là trạng thái nhiệt động học lý tưởng của vật chất, trong đó mọi chuyển động nhiệt đều ngừng.
- Nhiệt độ không tuyệt đối được tính là 0 K trong Nhiệt giai Kelvin.
Đơn vị tính: Kelvin (K)
Chú thích:
: số mol chất .
: khối lượng chất .
: khối lượng 1 mol chất .
: thế tích khí ở điều kiện tiêu chuẩn
Chú thích:
: số mol chất .
: thế tích khí .
: hằng số các khí 8,31 .
: áp suất của chất khí
: nhiệt độ .
Định nghĩa quá trình đẳng nhiệt:
Là quá trình thay đổi trạng thái chất khí, nhưng nhiệt độ được giữ nguyên không đổi.
Phát biểu:
Quá trình đẳng nhiệt là quá trình thay đổi trạng thái chất khí, nhưng nhiệt độ được giữ nguyên không đổi.
Trong quá trình đẳng nhiệt thì thể tích và áp suất tỉ lệ nghịch với nhau.
Chú thích:
: áp suất chất khí
: thể tích chất khí
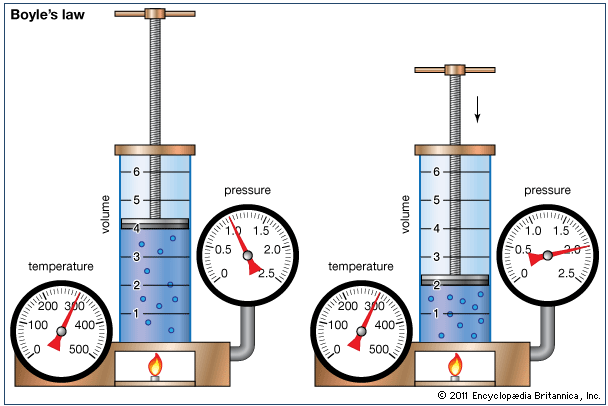
Nhiệt độ được giữ nguyên, khi thể tích giảm thì áp suất tăng.
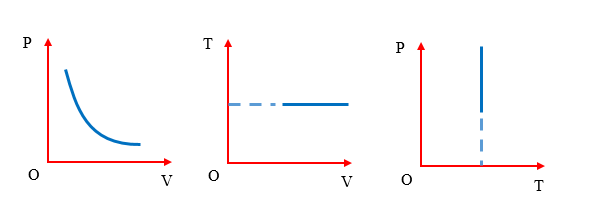
Đồ thị của quá trình đẳng nhiệt.
Chú thích:
: số mol chất .
: thế tích khí .
: hằng số các khí 8,31 .
: áp suất của chất khí
: nhiệt độ .
Định nghĩa quá trình đẳng nhiệt:
Là quá trình thay đổi trạng thái chất khí, nhưng nhiệt độ được giữ nguyên không đổi.
Phát biểu:
Quá trình đẳng nhiệt là quá trình thay đổi trạng thái chất khí, nhưng nhiệt độ được giữ nguyên không đổi.
Trong quá trình đẳng nhiệt thì thể tích và áp suất tỉ lệ nghịch với nhau.
Chú thích:
: áp suất chất khí
: thể tích chất khí

Nhiệt độ được giữ nguyên, khi thể tích giảm thì áp suất tăng.

Đồ thị của quá trình đẳng nhiệt.
Hãy giúp Công Thức Vật Lý chọn lọc những nội dung tốt bạn nhé!